Hogyan működik a CBD?

Mindannyian tudjuk, hogy a kannabisz THC-t, azaz delta 9-tetrahidrokannabinolt tartalmaz. Ez az a jól ismert kannabinoid, ami a bódulatért, utcai nyelven a „betépésért” felelős, illetve az olyan közismert gyógyászati hatásokért, mint a hányinger- és fájdalomcsillapítás és az étvágyfokozás.
A kannabisz termesztők elsődleges célja, hogy a fogyasztók minél erősebb bódulatot érezzenek és ezért általában olyan fajtákat termesztenek, amikben a lehető legmagasabb a THC tartalom. A kutatók kannabisz növénnyel végzett vizsgálataiból ismert, hogy a kannabiszban nagyjából 140 kannabinoid van, tehát az, hogy a nagyközönség ezek közül csak az egyiket ismeri, őrültségnek tűnhet.
A mai világban a kannabisz kultúra gyorsan növekszik, a világ minden táján úttörő tudományos vizsgálatokat végeznek és megtanuljuk, hogy sokkal több felfedezni való van ebben a bámulatos növényben. A modern kutatások egyik legnagyobb felfedezése a második legkoncentráltabb kannabinoid – a kannabidiol (cannabidiol), rövidítve CBD. A THC és CBD a két legnagyobb mennyiségben előforduló kannabinoid a természetben.
A CBD olyan, mint a THC testvére és mint minden testvér néha szimbiózisban dolgoznak együtt, néha egymás ellen dolgoznak, néha pedig kiegészítik egymást. A CBD-vel ellentétben a THC egy pszichtróp vegyület (ami azt jelenti, hogy a központi idegrendszeren keresztül hatva befolyásolja az agyműködést, ami megváltozott hangulatot, viselkedést, érzékelést és megismerést eredményezhet) és aminek hatásait a felhasználók leginkább akkor érzik, amikor kannabiszt szívnak.
A „betépés” felelős az ellazult érzésért, az érzékek felerősítéséért és persze az elmaradhatatlan nassolásért, ami akkor következik be, mikor ránk tör a kannabisz okozta étvágy érzése. A THC-nak számos tünet esetében van gyógyászati hatása, többek között az enyhe és középsúlyos fájdalom, az álmatlanság, a depresszió, az émelygés és étvágytalanság, csak hogy néhányat említsünk. Egyes embereknél azonban a THC okozhat szorongást vagy paranoiát, ami gyakran kapcsolódik ahhoz az érzéshez, hogy az idő lelassul, ami természetesen nem igaz.
Ezzel szemben a CBD nem pszichtróp kannabinoidnak minősül, bár úgy tűnik, hogy rendelkezik némely pszichoaktív, például nyugtató hatással. A gyógyászati alkalmazásai széles körűek, ide tartozik a gyulladás, a hányinger, a szorongás, a depresszió, a reumás ízületi panaszok, az epilepsziás rohamok csökkentése vagy megelőzése, és a fájdalomcsillapító hatás akár olyan esetben is, amikor ezeket a tüneteket hagyományos gyógyszerekkel nehéz kezelni.
Mivel a CBD nem pszichotróp a betegek anélkül használhatják, hogy a „betépnének”, és képesek funkcionálni a munkahelyükön, kezelhetnek gépeket (például autót), és semmilyen tevékenységüket sem gátolja intoxikáció.
Bár a THC és a CBD egyénileg is rendelkeznek sok előnyös tulajdonsággal, együtt használva, ahogy a kannabisz növényben is vannak, hatásuk sokkal lenyűgözőbb. Amikor a THC mellett dolgozik, a CBD képes csökkentni azt a szorongást, amit esetenként a THC okozhat, és egyes esetekben hatékonyabb, ha együtt használják őket, különösen olyan emberek esetében, akiknek többféle tünetük van.
Az emlősök, a madarak, a hüllők és a halak mind állítanak elő endokannabinoid vegyületeket a testükben, amelyek alapvetően a „természetesen” termelt kannabinoidok, olyanok, mint a THC vagy a CBD. Az egyik ilyen neves belső kannabinoid vegyület az anandamid. Technikailag az anandamid (Ananda = boldogság szanszkrit nyelven + amid = kémiai típus) egy neurotranszmitter vegyület, amelyet igény esetén termel a testünk.
A THC és az anandamid is kannabinoid receptorokon keresztül hatnak, amelyek a testünk egészében megtalálható sejtek felületén helyezkednek el, és hasonló hatással vannak olyan dolgokra, mint például a fájdalom, az étvágy és a memória. A receptorok csupán sejtekbe ágyazott kapuőrző fehérjék, amelyek külső molekulákból közvetítenek kémiai jeleket a sejtbe, közölve, hogy azok csináljanak valamit, olyanok, mint a sejtjeink légiforgalmi irányítói, de ez a kommunikáció csak akkor történik meg, miután egy molekula vagy vegyület kötődik hozzájuk. Egy molekula, amely egy receptorhoz kötődik, az úgynevezett ligandum és a receptorok nagyon specifikusak abban, hogy mi képes kötődni hozzájuk, tehát csak bizonyos vegyületek kötődnek egyes típusú receptorhoz.
Olyan ez, mint a kulcs és a zár, csak bizonyos kulcsok nyitnak ki egyes ajtókat és amikor az ajtó nyitva, létrejön egy átjáró. Ez az átjáró a receptorok esetében egy irányított jel. Egyetlen sejten sok különböző típusú receptor lehet, amelyek különböző vegyületekkel való kommunikációhoz készültek.
A kannabinoidok csak azért vannak hatással ránk, mert a testünk tartalmazza ezeket a receptorokat, amelyek pedig azért készülnek, hogy specifikus kannabinoid molekulák kötődjenek hozzájuk. Az emberi agy valójában több kannabinoid receptort tartalmaz, mint bármely más G-fehérje-kapcsolt receptort! Az a tény, hogy a sejtjeink ilyen sok receptort tartalmaznak, amikhez kifejezetten a kannabiszból származó kannabinoidok, valamint a testünk által termelt „belső kannabinoidok” (endokannabinoidok) kötődnek, magyarázatul szolgálhat arra, hogy az emberek miért vonzódnak úgy ehhez a növényhez.
Nincs semmi természetellenes abban, hogy a testünk hasznosítja a kannabinoidok okozta folyamatokat. A kannabisz egy igen hatékony természetes gyógyszernek bizonyul, aminek rendelkezésre kell állnia azoknak a betegnek, akiknek szükségük van rá.
Eddig két ismert kannabinoid receptort találtak a testünkben (újabb jelöltek vannak kutatás alatt), amelyekhez kötődik a THC; a CB1 receptorok, amelyek leginkább az agyban és a központi idegrendszerben találhatók, és a CB2 receptorok, amelyek az egész testben eloszlanak, de többnyire az immunrendszerben találhatók. A kannabiszban található kannabinoidok és a testünk által természetesen termelt endokannabinoidok mellet sok egyéb anyag van, amelyek kisebb mértékben befolyásolják az endokannabinoid rendszert, mint például; az Echinacea (kasvirág), a kurkuma, a fekete bors, a kakaó stb. Ezekről és néhány egyéb fogyasztható anyagról is megállapították, hogy kötődnek ugyanazokhoz a kannabinoid receptorokhoz.
A CBD az elmúlt években jelentős érdeklődést váltott ki a tudósok és az orvosok körében – de a CBD molekuláris szinten gyakorolt terápiás hatása még mindig tisztázatlan. A kannabidiol egy pleiotróp gyógyszer, mivel számos molekuláris útvonalon számos hatást fejt ki. A tudományos irodalom több mint 65 molekuláris célpontot azonosított a CBD esetében.
Bár a CBD kis affinitással kötődik a két kannabinoid receptorhoz (CB1 és CB2), számos nem-kannabinoid receptort és ioncsatornát modulál. A CBD különböző receptorfüggetlen úton is működik – például az endogén neurotranszmitterek (mint például az anandamid és az adenozin) „újrafelvételének” késleltetésével és bizonyos G-fehérjéhez kapcsolt receptorok kötődési hatásának fokozásával vagy gátlásával.
A legújabb tanulmányok kimutatták, hogy a CBD több mint 65 receptorra hat, és potenciális farmakológiai hatásai közé tartozik a nyugtató, fájdalomcsillapító, szorongásoldó, antioxidáns, valamint a gyulladás gátlása, valamint az érrendszeri simaizomsejtek és endoteliális sejtek rendellenes proliferációja és apoptózisa.
Íme néhány módszer, amellyel a CBD terápiás hatást gyakorol:
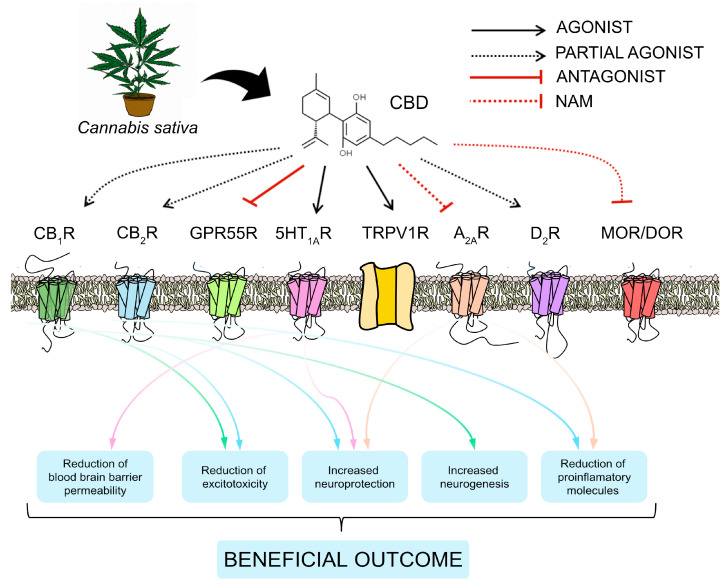
A CBD jótékony hatásai a különböző receptorokra gyakorolt hatásán keresztül.
A CBD fő molekuláris célpontjainak sematikus ábrázolása 2024-ben:

Szerotonin receptor
Jose Alexandre Crippa és kollégái a San Paulo Egyetemen Brazíliában és a Királyi Egyetemen Londonban úttörő kutatást végeztek CBD-vel és az idegrendszeri összefüggéseket mutató szorongással. Magas koncentrációban a CBD közvetlenül aktiválja az 5-HT1A (hidroxi-triptamin) szerotonin-receptort, ezáltal szorongásgátló hatást vált ki. Ez a G-kapcsolt fehérje receptor számos biológiai és neurológiai folyamatban vesz részt, beleértve (de nem kizárólagosan) a szorongást, a függőséget, az étvágyat, az alvást, a fájdalomérzetet, a hányingert és a hányást.
Az 5-HT1A az 5-HT receptorok családjába tartozik, melyeket a szerotonin nevű neurotranszmitter aktivál. Mind a központi, mind a perifériás idegrendszerben megtalálható 5-HT receptorok kémiai üzenetek különböző intracelluláris kaszkádjait kiváltják, hogy az üzenet kémiai kontextusától függően serkentő vagy gátló választ adjanak.
Egy nemrégiben végzett tanulmányban kimutatták, hogy a szorongásoldó hatás mellett a CBD fájdalomcsillapító hatását részben szintén az 5-HT1A receptorok közvetítik.
A CBDA (kannabidiolsav), a CBD nyers, hevítetlen változata a növényben, szintén erős affinitással van a 5-HT1A receptorra, még erősebbel, mint a CBD. A preklinikai vizsgálatok azt mutatják, hogy a CBDA egy erős antietikum, erősebb, mint a CBD vagy THC, amelyek szintén hányinger-ellenes tulajdonságokkal rendelkeziknek.
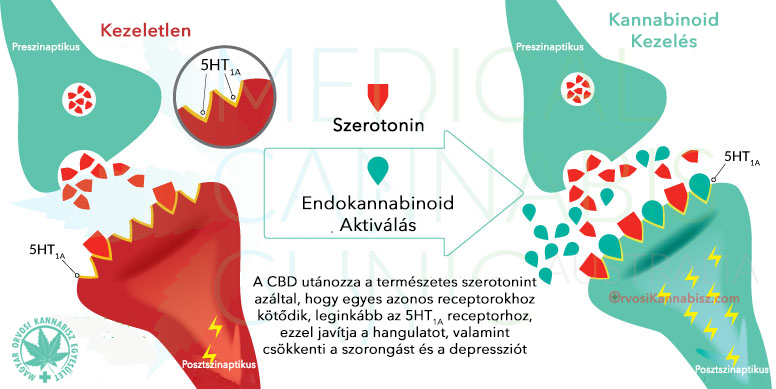
CBD és szorongás
Vanilloid receptor
A CBD közvetlenül kölcsönhatásba lép különböző ioncsatornákkal, amivel terápiás hatás fejt ki. A CBD például kötődik a TRPV1 receptorokhoz, amelyek szintén ioncsatornákként működnek. A TRPV1-ről ismert, hogy a fájdalomérzetet, a gyulladást és a testhőmérsékletet közvetíti.
A TRPV a „tranziens receptor potenciál kationcsatorna alcsalád V” technikai rövidítése.
A tudósok a TRPV1-et „vanilloid receptornak” nevezik, az ízletes vanília bab után. A TRPV1 több tucat TRP (kiejtve „trip”) receptor variáns vagy alcsalád egyike, amely a gyógynövények széles körének hatásait közvetíti. A vanília eugenolt tartalmaz, ami egy antiszeptikus és fájdalomcsillapító tulajdonságokkal rendelkező illóolaj és a véredények tisztításában is segít. Történelmileg a vanília babot népi gyógymódként használták fejfájás ellen.
A CBD kötődik a TRPV1-hez, ami befolyásolhatja a fájdalomérzetet. Egy nemrégiben végzett tanulmányban kimutatták, hogy a CBD fájdalomcsillapító hatását a TRPV1 receptorok közvetítik.
A kapszaicin – a chili paprikában lévő csípős vegyület – aktiválja a TRVP1 receptort. Az endogán kannabinoid, az anandamid is TRPV1 agonista.
A CBD antiepileptikus hatásait a vanilloid 1 receptor közvetíti
A legfrissebb kutatási adatok erősen utalnak a TRPV1 szerepére a CBD antikonvulzív hatásának lehetséges mechanizmusaiban. A nagy dózisú CBD antikonvulzív hatásának részleges gátlása a TRPV1 knockout egerekben jelezheti a TRPV1-től eltérő célpontok érintettségét.
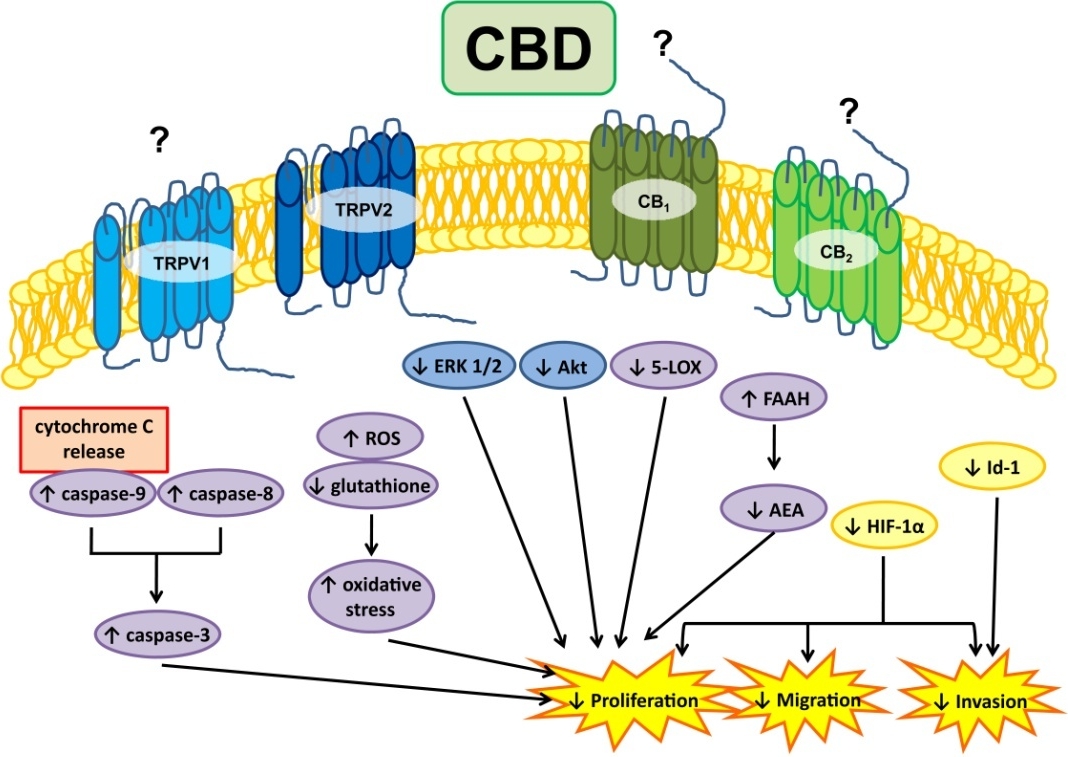
CBD és glióma (agydaganat)
G-protein kapcsolt „árva” receptorok
A G-protein kapcsolt receptorok családjában található árva receptorok hasonló struktúrával rendelkeznek, mint más azonosított receptorok, de az endogén ligandumot, azt a vegyületet, ami belsőleg termelődik és kapcsolódik hozzá, még nem azonosították, ezért a tudósok még mindig nem biztosak abban, hogy egy nagyobb receptorcsoporthoz tartozik-e. Ezek a receptorok a GPR rövidítést kapták.
GPR55
Míg a kannabidiol közvetlenül aktiválja az 5-HT1A szerotoninreceptort és több TRPV ioncsatornát, egyes vizsgálatok azt mutatják, hogy a CBD antagonistaként funkcionál, azaz blokkol vagy deaktivál egy másik G-fehérje-kapcsolt receptort, a GPR55-t. A GPR55 nagy számban található meg az agyban, különösen a kisagyban. A különféle fiziológiai folyamatok között részt vesz a vérnyomás és a csontsűrűség befolyásolásában.
A GPR55 elősegíti az oszteoklaszt sejtek működését, így megkönnyíti a csontok reabszorpcióját (felszívódását). A túlzott GPR55 receptor jelátvitel csontritkulással jár.
A GPR55, amikor aktiválva van, elősegíti a rákos sejtek proliferációját (burjánzását), egy 2010-es tanulmány szerint, amit a Kínai Tudományos Akadémia (Chinese Academy of Sciences) kutatói végeztek Shanghaiban. Ez a receptort különféle ráktípusokban is megtalálható.
A CBD egy GPR55 antagonista (blokkoló), ahogy azt az Aberdeni Egyetem kutatója, Ruth Ross jelentette a Nemzetközi Kannabinoid Kutató Társaság konferenciáján 2010-ben a svédországi Lundben. A GPR55 jelzés blokkolásával a CBD csökkentheti a csontfelszívódást és a rákos sejtek proliferációját.
GPR3 és GPR6
Korábban arról számoltak be, hogy a GPR3 szerepet játszik az Alzheimer-kórban, míg a GPR6 potenciális szerepet játszik a Parkinson-kórban. A GPR3-at és a GPR6-ot árva receptoroknak tekintik. A GPR3 és a GPR6 azonban filogenetikusan kapcsolódnak a kannabinoid receptorokhoz.
A Louseville Orvostudományi Egyetem munkatársai által szolgáltatott adatok azt mutatják, hogy a CBD a GPR3 és GPR6 receptor inverz agonistájaként működik. Eredményeik először mutatják be, hogy mind a GPR3, mind a GPR6 új molekuláris célpontok a CBD számára. A felfedezés, hogy a CBD egy új inverz agonistaként működik mindkét receptoron, azt jelzi, hogy a CBD lehetséges terápiás hatásai (például az Alzheimer-kór és Parkinson-kór kezelésében) ezen fontos receptorokon keresztül közvetíthetők.
GPR12
A GPR12 olyan fiziológiai folyamatokban vehet részt, mint például az oocita meiotikus meggátlása és az agy fejlődésének fenntartása, valamint olyan patológiás állapotok, mint például a metasztatikus rák. Ugyancsak a Louseville Orvostudományi Egyetem kutatói állípították meg, hogy a CBD fordított agonistaként működik a GPR12 receptoron, ami tehát új molekuláris cél a CBD számára. A CBD ígéretes új terápiás szer a rák ellen, és a GPR12-ről kimutatták, hogy megváltoztatja az áttétes ráksejtek viszkoelasztikus tulajdonságait. Ez a felfedezés új mechanizmust biztosít a CBD számára, és egy olyan kezdeti kémiai alapzatot, amelyen a GPR12-re erősen ható és hatásos szerek fejleszthetők ki, melyek végső célja a rák metasztázisának blokkolása.
PPAR-ok – nukleáris receptorok
A CBD rákellenes hatást fejt ki a PPAR-ok [peroxiszóma proliferátor aktiválta receptorok] aktiválásával is, amelyek a sejtmag felszínen találhatók. A PPAR-gamma néven ismert receptor aktiválásának anti-proliferatív (burjánzást gátló) hatása van, valamint képes tumor regressziót indukálni humán tüdőrák sejtvonalakban. A PPAR-gamma aktivációja degradálja az amiloid-béta plakkot, ami egy kulcsfontosságú molekula az Alzheimer-kór kifejlődésében. Ez az egyik oka annak, hogy a CBD, ez a PPAR gamma agonista (aktiváló), hasznos gyógyír lehet Alzheimer-betegek számára.
A PPAR receptorok azokat a géneket is szabályozzák, amelyek részt vesznek az energia homeosztázisban, a lipid felvételben, az inzulinérzékenységben és más anyagcsere funkciókban. A cukorbetegeknek, ennek megfelelően, előnyös lehet a CBD-dús kezelés.
A PPAR-alfa receptor CBD enzim-közvetített aktiválásának antipszichotikus hatása lehet. Annak a génnek a polimorfizmusa vagy mutációja, ami a PPAR-alfa-t kódolja, hiányos PPAR-alfa jelzést eredményezhet, amelyet összefüggésbe hoztak a skizofréniával. A PPAR-alfa aktiválása gyulladásgátló és csökkenti a dopamin felszabadulását, ezáltal minimalizálja a skizofrén tüneteket.
A CBD, mint alloszterikus modulátor
A CBD egy alloszterikus receptor modulátorként is funkcionál, ami azt jelenti, hogy növelheti vagy gátolhatja azt, ahogy egy receptor továbbít egy jelet, azáltal hogy megváltoztatja a receptor formáját.
A CBD rendkívül alacsony affinitással van a CB1 receptorokra, de valamelyest befolyásolhatja őket. Kanadai kutatók kimutatták, hogy a CBD a kannabinoid CB1 receptor „negatív alloszterikus modulátora”, amely az agyban és a központi idegrendszerben koncentrálódik. Bár a kannabidiol nem közvetlenül a CB1 receptorhoz kötődik, mint a THC, a CBD alloszterikusan lép kölcsönhatásba a CB1-gyel, és megváltoztatja a receptor formáját oly módon, hogy gyengíti a CB1 THC-val való kötődését – ezért az emberek nem érzik „betépve” magukat CBD-dús kannabisz használatakor úgy, mint amikor THC-dús gyógynövényt fogyasztanak. A CBD-dús, kevés THC-t tartalmazó termékek anélkül szolgáltathatnak terápiás előnyöket, hogy eufórikus vagy diszfóriás hatásuk lenne.
Egyszerűen szólva a CBD részben hatástalanítja a THC pszichotróp hatásait.
Az ausztrál tudósok arról számoltak be, hogy a CBD a GABA-A receptor „pozitív alloszterikus modulátoraként” működik. Más szavakkal, a CBD kölcsönhatásba lép a GABA-A receptorral olyan módon, hogy fokozza a receptor kötődési affinitását a fő endogén agonista, a gamma-aminobu-vajsav (GABA) számára, ami a legfőbb inhibitor (gátló) neurotranszmitter az emlősök központi idegrendszerében. A Valium és más Benzo nyugtatók hatását a GABA receptor jelátvitel közvetíti. A CBD csökkenti a szorongást a GABA-A receptor alakjának megváltoztatásával úgy, hogy a GABA természetes nyugtató hatását fokozza.
CBD, az újrafelvétel gátló
Hogyan képes a CBD, egy külső növényi vegyület, bejutni egy emberi sejtbe és kötődni egy nukleáris (sejtmag) receptorhoz? Először át kell haladnia a sejtmembránon, úgy hogy felveteti magát egy zsírsavkötő fehérjével (FABP), ami különböző lipid molekulákat kísér a sejt belsejébe. Ezek az intracelluláris szállító molekulák azok, amik a tetrahidrokannabinolt (THC) és az agy saját kannabiszszerű molekuláit, az anandamid és 2AG endokannabinoidokat átkísérik a membránon keresztül, a sejten belül található több célállomáshoz. A CBD és a THC egyaránt modulálják a mitokondiumok felszínén és a sejtmagban található receptorokat.
A CBD-nek, mint kiderült, erős affinitása van háromféle FABP-val, és ugyanazokért a szállító molekulákért versenyez az endokannabinoidokkal, amelyek zsírsavak. Az anandamidot a sejt belsejébe kerülve a FAAH [zsírsav-amid-hidroláz] bontja le, egy metabolikus enzim, ami természetes részét képezi a molekuláris életciklusnak,de a CBD zavaja ezt a folyamatot azáltal, hogy csökkenti az anandamid hozzáférését a FABP szállító molekulákhoz és késlelteti az endokannabinoid bejutását a sejt belsejébe.
A CBD gátló hatása azt jelenti, hogy több anandamid marad a szervezetben és hosszabb ideig.
A Stony Brook Egyetem tudósai szerint a CBD egy anandamid újrafelvétel és lebontás gátlóként működik, ezáltal megemeli az endokannabinoid szintet az agy szinapszisaiban. Az endokannabinoid tónus fokozása az újrafelvétel gátlásával, kulcsfontosságú mechanizmus lehet, amellyel a CBD neuroprotektív hatásokat fejt ki görcsrohamok ellen, valamint számos más egészségügyi előnyöket.
Az anandamid olyan alapvető funkciókat segít szabályozni, mint az öröm és a jutalom, az étvágy, az ovuláció, a feledékenység, az alvás és a fájdalom.
A CBD és az anandamid kapcsolata nagy szerepet játszhat abban, hogy a jövőben jobban megértsük a szorongást. Egy a New York Timesban megjelent tanulmányi áttekintés szerint a betegek kevésbé szoronganak, amikor több anandamid van a szervezetükben. Mivel a CBD gátolja az enzimet, amely lebontja az anandamidot, ez lehetővé teszi, hogy több legyen ebből a jó érzést keltő vegyületből a testben.
A több anandamid, nagyobb CB1 aktiválást jelent, mivel a THC-hoz hasonlóan az anandamid előnyben részesíti ezt a leginkább az agyban található receptort, így kevesebb átjárót hagy a THC kötődéséhez az említett receptorokon, és ezzel csökkenti annak pszichotróp hatását. Ez azonban nem azt jelenti, hogy a THC-nak így a gyógyhatásai is csökkenek, hiszen az kötődik még a CB2 receptorokhoz is, amik a CB1 receptorral ellentétben nem okoznak pszichotróp hatást, viszont sok olyan mechanizmusért felelősek, amik széleskörű gyógyhatásokat biztosítanak.
Míg a THC-ról ismert, hogy növeli az étvágyat, a CBD ellenkező hatást vált ki, hasonlóan a vitatott elhízás elleni gyógyszerhez, a Rimonabant-hoz.
A CBD serkenti a 2-AG kibocsátást is, egy másik endokannabinoidét, amely aktiválja a CB1 és CB2 receptorokat.
Adenozin receptor
A CBD szorongásoldó tulajdonságai részben az úgynevezett adenozin receptorok aktiválásának tulajdoníthatók. Ezek a receptorok jelentős szerepet játszanak a szív- és érrendszeri funkciókban, a szívizom oxigén fogyasztás szabályozásában és a koszorúér vérátáramlásban, ezzel megmagyarázzák sok olyan szorongással járó tünet kialakulását, mint a feszült, szorító érzés a mellkasban, légszomj stb. Ezek a receptorok olyan más agyi neurotranszmitterek szabályozói, mint a dopamin és a glutamát. A dopamin nem csak kellemes érzések előidézéséért felelős, de hatással lehet az alvásra, a hangulatra, a memóriára, a figyelemre és az akaratlagos mozgásra. Más kábítószerek, mint a kokain és a metamfetamin szintén felerősítik a dopamin receptorok hatásait, de sokkal nagyobb mértékban. Míg THC ideiglenesen növeli a dopamin szintet, a CBD nem.
A CBD gyulladásgátló és szorongásellenes hatásai részben annak tulajdonítható, hogy gátolja az adenozin-újrafelvételt. Ennek a neurotranszmitternek a felvételét késleltetve, a CBD fokozza az adenozin szintjét az agyban, ami növeli az adenozin receptor aktivitását. Az A1A és A2A adenozin receptorok jelentős szerepet játszanak a szív- és érrendszer működésében, a szívizom oxigén fogyasztásának és a koszorúér vérátáramlásának szabályozásával. Ezeknek a receptoroknak széleskörű gyulladáscsökkentő hatásaik vannak az egész szervezetben.
Az adenozin receptor széleskörű gyulladáscsökkentő hatásokkal is rendelkezik.
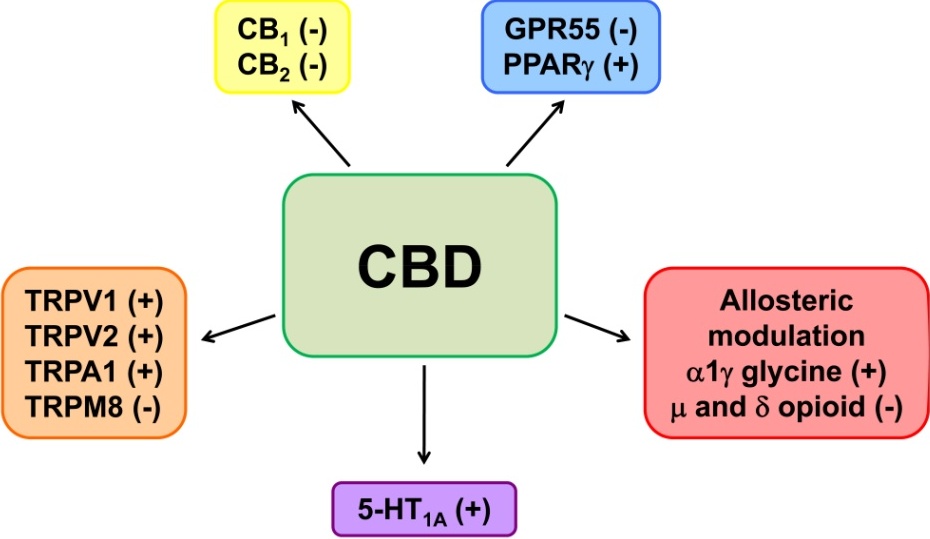
A CBD hatásmechanizmusai
Az ID-1 gén
Dr. Sean McAllister kutatásai a san franciscoi Pacific Medical Centerben azt mutatták, hogy a CBD csökkenti a mellrák sejtburjánzást, inváziót és metasztázist az ID-1 gén expresszió gátlásával. Bővebben az erről szóló cikkben lehet olvasni:
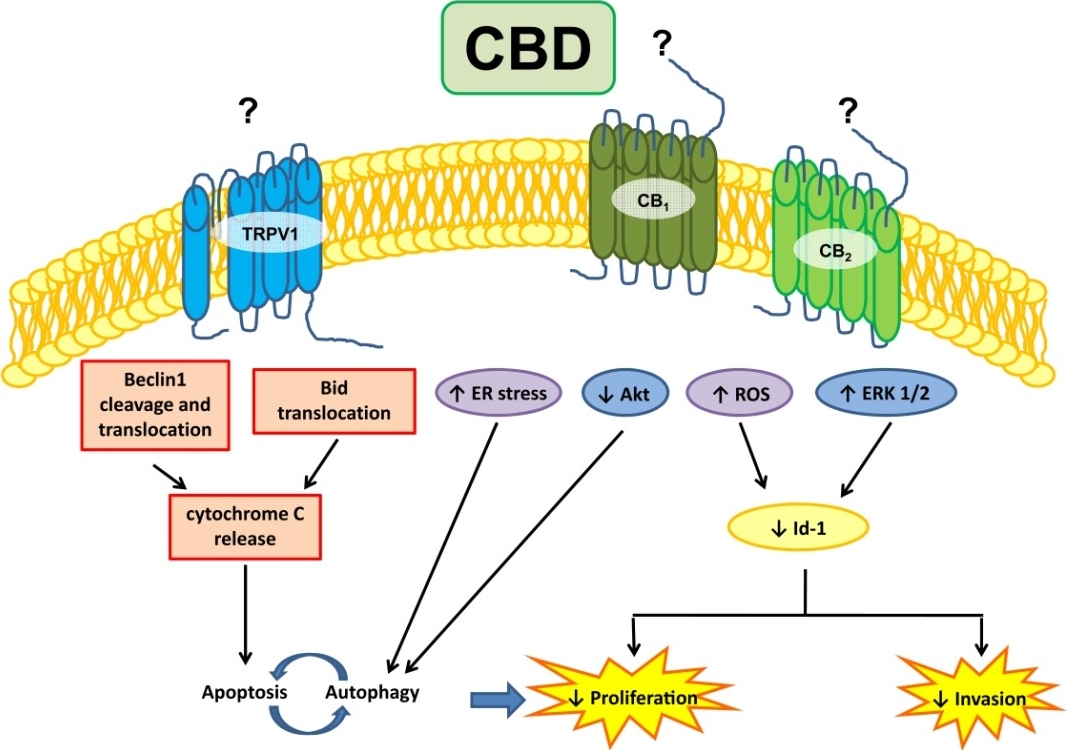
CBD és mellrák
CBD és Epilepszia – A GABA receptor
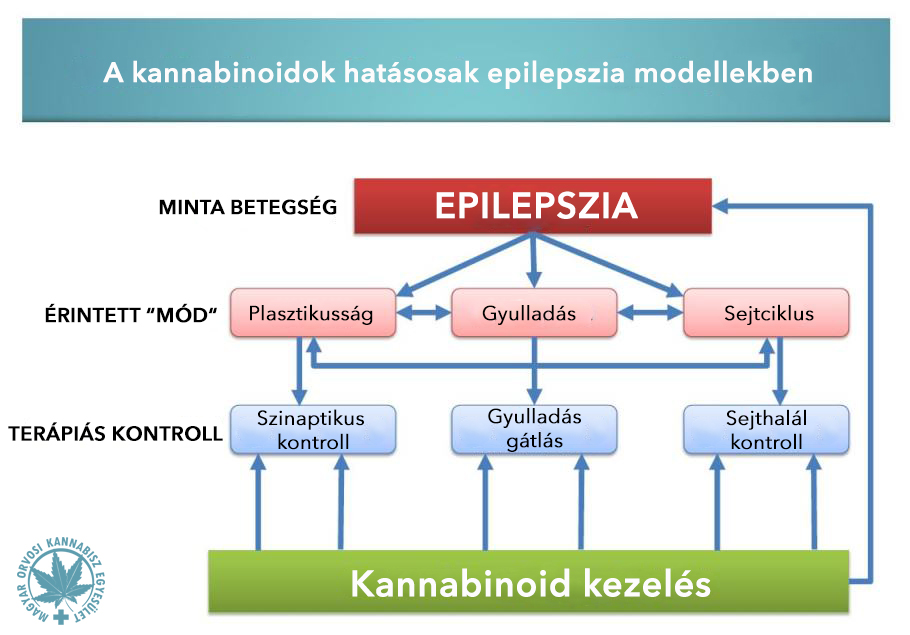
Ahogy azt az anekdotikus történetek egyre nyilvánvalóbbá teszik, az endokannabinoid-rendszer szerepet játszik az epilepszia kezelésében.
Az egyik módja annak, ahogy a CBD csökkenti a rohamokat, az a GABA nevű neurotranszmitterre kifejtett hatása. A GABA egy nyugtató hatású vegyület, ami csillapítja az ingerlékenységet az agyban. Ha a GABA szintje túlságosan lecsökken, akkor nagyobb a valószínűsége egy roham kialakulásának. A CBD egy GABA-felvétel inhibitor, ami azt jelenti, hogy a CBD jelenlétében megnövekszik a GABA mennyisége az agyban.
Ausztrál kutatók arról számoltak be, hogy a CBD a GABA-A receptor „pozitív alloszterikus modulátorként” működik. Más szóval, a CBD oly módon lép kölcsönhatásba a GABA-A receptorral, hogy fokozza a receptor affinitását annak fő endogén agonistájával, a gamma-amino-vajsavval (GABA), amely a fő gátló neurotranszmitter az emlősök központi idegrendszerében. A Valium és más Benzodiazepinek nyugtató hatását a GABA receptor átvitel közvetíti. A CBD úgy csökkenti a szorongást, hogy olyan módon változtatja meg a GABA-A receptor alakját, amely felerősíti a GABA természetes nyugtató hatását.
A THC és a CBD egyaránt gátolják a szinaptikus ingerületátvitelt, vagy megváltoztatják azt ahogy az agyban lévő neuronok más vegyületeket kibocsátanak és elnyelnek. A CBD-ről azt is kimutatták, hogy képes növelni más gyakran használt antiepileptikumok hatékonyságát és neuroprotektív tulajdonságairól is ismert. Segít megőrizni az agysejtek egészségét és csökkenti a sejtkárosodást.
(A THC közvetve növeli a dopamin szintjét azáltal, hogy gátolja GABA-t. GABA általában visszafogja a nucleus accumbensbe felszabaduló dopamin mennyiségét. Azonban, amikor a THC blokkolja a GABA-t, a felszabadult dopamin mennyisége megnövekszik.)
A GABA rohamokban betöltött szerepe csak egy kis darabja a bonyolult epilepszia puzzle-nek. További kutatásokra van szükség, hogy teszteljék a CBD hatásosságát különböző típusú epilepsziákban. Ahogy egyre többet tudunk meg a működéséről, biztos, hogy további hatásmechanizmusokat fogunk felfedezni.
Példák arra, hogy a CBD hogyan állítja meg a rohamokat:
- A CBD blokkolja az NMDA receptort (hasonló mechanizmussal mint a Felbamát)
- A CBD fokozza a GABA receptort (hasonló mechanizmussal mint a Felbamát, a Depakote, a Tegretol, az Onfi, a Fenobarbitál)
- A CBD stabilizálja az ioncsatornákat (hasonló mechanizmussal mint a Banzel, a Lamictal, a Dilantin, a Keppra,
a Trileptal)
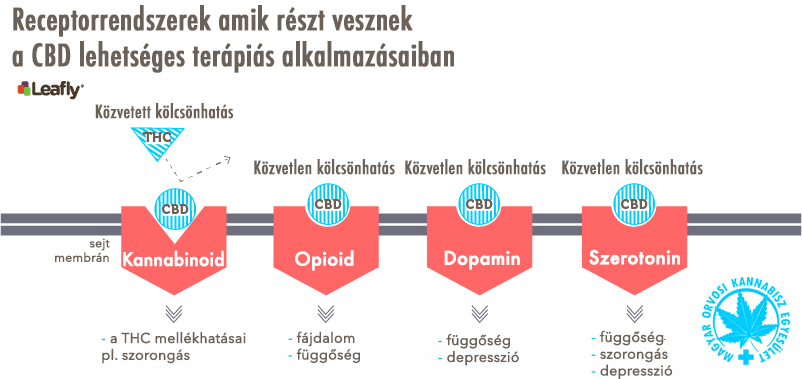
A CBD több különböző receptor rendszerrel lép közvetlenül, vagy közvetve kölcsönhatásba az agyban. Közvetve befolyásolja a fő kannabinoid receptort az agyban, azáltal hogy csökkenti a THC azon képességét, hogy az aktiválja ezt a receptort. Számos egyéb receptorral is kölcsönhatásba lép. Ezeknek egy része itt látható. Minden vörös forma különböző receptort jelent az agyban, amely megtalálható egy idegsejten. A CBD néhány lehetséges terápiás alkalmazása, ami a receptor rendszerrel való kölcsönhatáshoz társítható, az egyes receptorok alatt van felsorolva.
Erős antioxidáns
A CBD egy erős antioxidáns, ami enyhíti a szabad gyökök negatív hatását. A nagyon reaktív szabad gyökök akkor keletkeznek, amikor oxigént használunk az élelem üzemanyagként való elégetéséhez.
Jelentős mennyiségű adat utal arra, hogy sok öregedéssel járó probléma abból fakad, hogy a szervezet nem képes megvédeni magát a szabad gyökök által kiváltott gyulladásos és oxidatív stressz ellen, amely termékeny talajt biztosít a neurodegeneratív és más időskori megbetegedések kialakulásához.
Tudományos körökben úgy tartják, hogy a szív- és érrendszeri megbetegedéseket, az autoimmun betegségeket, a neurológiai rendellenességeket, a rákot és magát az öregedés folyamatát a szabad gyökök okozzák. A szabad gyökök érintettek a fehérje amyloid plakkok kialakulásában, amelyek megtámadják a neurális szinapszisokat és megakadályozzák a normál kémiai és elektromos jelátvitel aktivitást az agyban.
Azáltal, hogy a szabad gyökökhöz kötődnek, az antioxidánsok képesek megtörni a plakk-képződés ciklust, ami az Alzheimer-kór kialakulásához kapcsolódik. Számos tanulmány kimutatta, hogy a CBD blokkolja az Alzheimer plakk képződést egy olyan mechanizmussal, amiben nincs szerepe a kannabinoid receptoroknak.
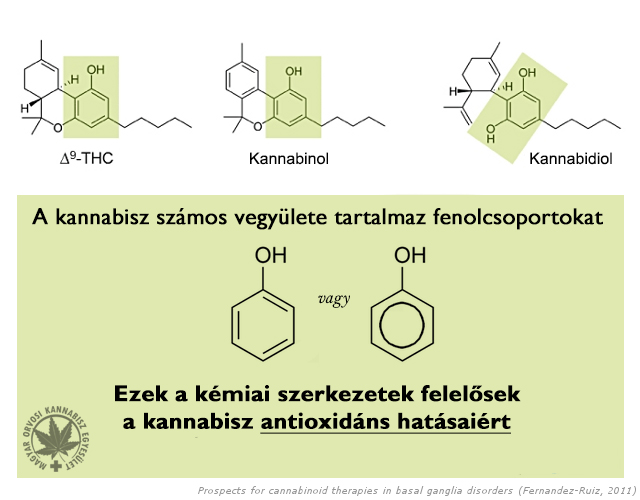
A CBD antioxidáns tulajdonságai meghaladják a C-vitamin és az E-vitamin antioxidáns hatóerejét.
THC-val kombinálva a CBD antioxidáns tulajdonságai még erősebbek.
Ismételten, a teljes növényi kannabisz-terápiák hatákonyabbak, mint a növény egyéni gyógyhatású vegyületeinek összessége.
Ellentétben azzal, ahogy egyesek vélekednek, egy növényből csak akkor lesz CBD-dús növény, ha rendelkezésre áll a genetikai felépítés, ami ezt biztosítja. A THC, a CBD és minden egyéb kannabinoid aránya genetikailag előre meghatározott. Az, hogy nagyon kevés magas CBD-t termelő növény (minden ami 4% feletti) van, egy szerencsétlen helyzet, ez a növények több éves magas THC tartalomra való keresztezésének közvetlen eredménye.
A ma elérhető mag készletek csupán 25-30%-a potenciálisan CBD-dús fajta (azaz >4%). Amikor ezek a fajták magokat teremnek, azok a magok különböző fenotípusú palántákat fognak sarjadzni, minden generációban lesz CBD-dús és THC-dús növény is. Átlagosan egy minden négy CBD-dús kannabisz növényből származó mag hoz létre CBD-dús fenotípusú palántát. Még a legritkább esetekben is csak kettő a négyből lesz az arány, így minden esetben 25-50% CBD-dús palánta lehetséges. Az egyetlen módja annak, hogy könnyen szaporítsunk egy a CBD-dús fajtát, ha találunk egy ilyen domináns fenotípust és anyanövényt nevelünk belőle, amiről klónokat metszünk. Az összes klón pontosan ugyanazt a THC:CBD arányt tartalmazza, mint az anya vagy a donor növény.
Honnan tudhatjuk, hogy egy kannabisz fajta CBD-dús? Vannak olyan kémiai vegyületekkel végzett tesztek, amik vegetatív növényekből azonosítják a CBD-dús jellemzőkkel rendelkező palántákat. Ezek a tesztek lehetőséget adnak a termesztőknek, hogy betekintést kapjanak a THC:CBD arányokba anélkül, hogy megvárnák a szüretelést és letesztelnék a virágokat/rügyeket.
Amikor leszüreteltük a virágmintát, amit kannabinoid tartalomra szeretnénk tesztelni, alapvetően két vizsgálati módszert alkalmazhatunk; mennyiségi vagy minőségi. Akár házi teszt készletet is vásárolhatunk, melyek közül vannak, amik már egészen pontos méréseket tudnak végezni.
Magok vásárlása esetén a mag árusítója, vagy a kannabisz fajta nemesítője által kiadott információkra tudunk hagyatkozni. Egyes esetekben a THC és a CBD aránya (1:2, 1:1, 2:1 stb.) van megadva, máskor a %-os mennyiség (20% THC, 6% THC / 6% CBD stb.), amit várhatóan az adott növény virága termel.
Kérünk mindenkit, támogassa non-profit egysületünk munkáját, akár csak egy pohár kávé árával.
Ezen az oldalon lehet támogatást küldeni:
https://orvosikannabisz.com/tamogatas/
Források:
http://www.thestonerscookbook.com/article/2015/04/16/everything-you-need-to-know-about-cbd/
https://www.projectcbd.org/how-cbd-works
http://www.beyondthc.com/wp-content/uploads/2012/07/CBDiary21.pdf
http://www.nytimes.com/2015/03/08/opinion/sunday/the-feel-good-gene.html?_r=0
Kutatások:
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3316151/
http://www.ncbi.nlm.nih.gov/pubmed/25666611
http://www.ncbi.nlm.nih.gov/pubmed/8874830
http://www.ncbi.nlm.nih.gov/pubmed/11606325
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3481537/
http://www.ncbi.nlm.nih.gov/pmc/articles/PMC3481531/
http://www.ncbi.nlm.nih.gov/pubmed/20565726
https://www.ncbi.nlm.nih.gov/pubmed/23488964
https://www.ncbi.nlm.nih.gov/pubmed/20829306
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC3079847/
https://www.ncbi.nlm.nih.gov/pubmed/14583744
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2874616/
https://www.ncbi.nlm.nih.gov/pubmed/25926795
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2095107/
https://www.ncbi.nlm.nih.gov/pubmed/23121618
https://www.ncbi.nlm.nih.gov/pmc/articles/PMC1575333/
https://www.ncbi.nlm.nih.gov/pubmed/25029033
https://www.ncbi.nlm.nih.gov/pubmed/24641282
http://pubs.acs.org/doi/abs/10.1021/acs.jmedchem.5b01824
https://www.ncbi.nlm.nih.gov/pubmed/26052038
https://www.ncbi.nlm.nih.gov/pubmed/26044547
https://www.ncbi.nlm.nih.gov/pubmed/26529344
https://www.ncbi.nlm.nih.gov/pubmed/26218440
https://www.ncbi.nlm.nih.gov/pubmed/26211948